la MAM – Matrice Adiposa Micronizzata - autologa
INTRODUZIONE
La matrice adiposa è il tessuto connettivo lasso che costituisce l’impalcatura del tessuto adiposo, al cui interno si trovano gli adipociti e una ricca frazione stromale (SVF), formata da vasi sanguigni, fibre (soprattutto collagene) e varie cellule. Gli adipociti sono organizzati in lobuli circondati da connettivi fibrosi e capillari che formano un microambiente ben vascolarizzato che nutre le cellule e le sostiene strutturalmente. Tra le principali cellule stromali troviamo: cellule progenitrici mesenchimali (ADMSCs, adipose-derived stem cells), periciti, cellule progenitrici endoteliali, cellule endoteliali, fibroblasti, macrofagi, linfociti, e preadipociti.
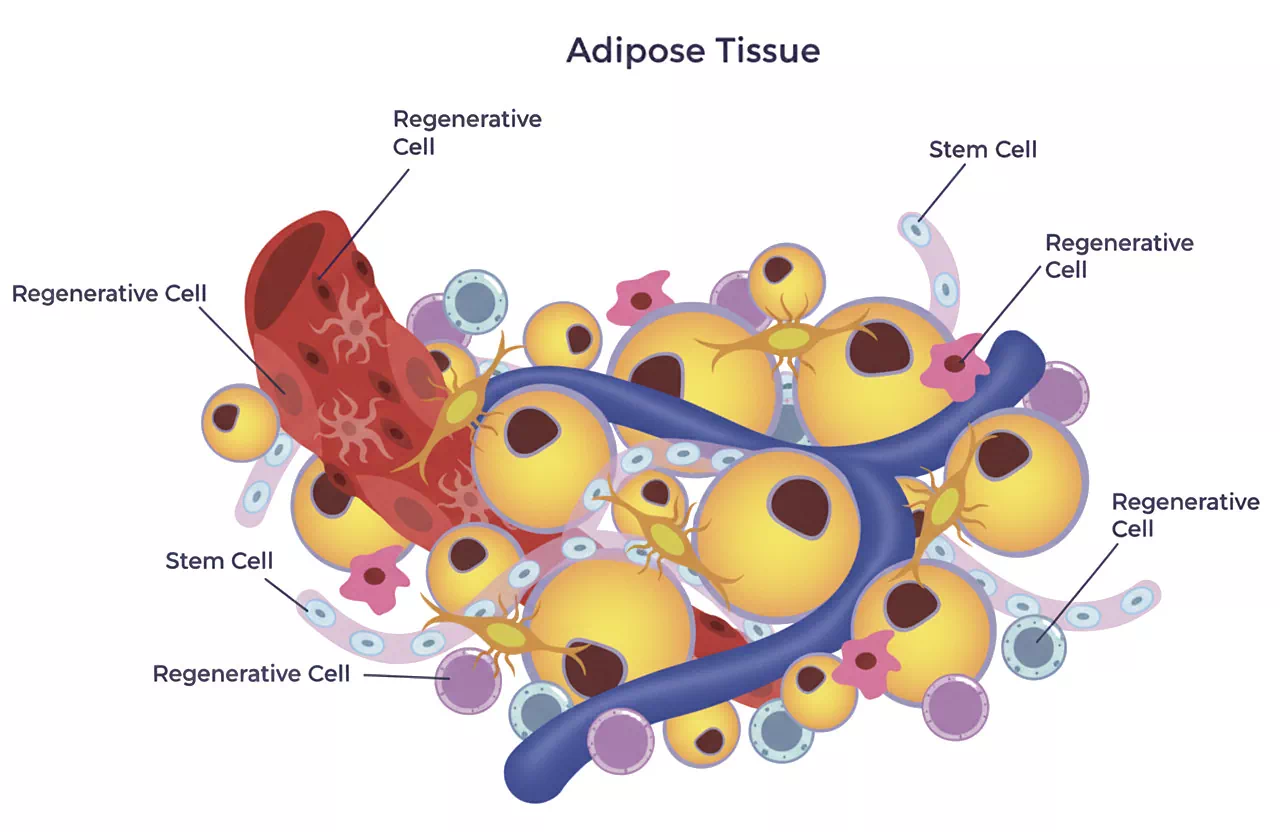
In sintesi, la matrice adiposa è la maggiore riserva di cellule rigenerative dell’organismo umano. Grazie alla sua composizione, il tessuto adiposo è coinvolto nella regolazione delle funzioni cellulari di molti organi attraverso diversi segnali endocrini, paracrini e autocrini. La ricchezza cellulare (da 500 a 2500 volte superiore al midollo osseo a parità di tessuto prelevato) e la presenza di un’ECM (extracellular matrix) vascolare fanno del tessuto adiposo una fonte molto interessante per applicazioni di medicina rigenerativa (Trivisonno et al. 2019; Copcu & Oztan 2020; Yaylacı et al. 2023; Arcani et al. 2025).
SVF: composizione e funzione
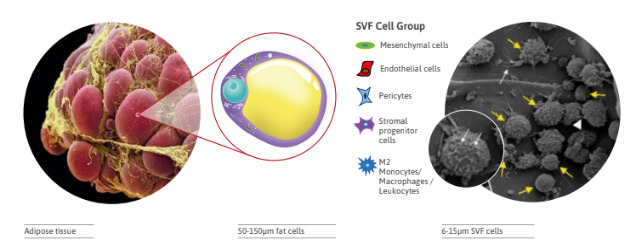
La frazione vascolo-stromale (SVF) è l’insieme eterogeneo di cellule non adipose e rappresenta circa il 15-20% delle cellule totali. Comprende: ADMSCs (circa il 10-15%), periciti, pre-adipociti, fibroblasti, cellule endoteliali e loro progenitori, globuli bianchi (es. macrofagi) e altre cellule del sangue. La SVF può essere ottenuta dal tessuto adiposo in due modi: tramite digestione enzimatica (con collagenasi, manipolazione estensiva non consentita) che libera le cellule dal loro substrato, oppure tramite metodi meccanici che frammentano il tessuto mantenendo però parte della matrice (tecnica di manipolazione minima consentita); in tal caso si parla di SVF tissutale (tSVF) anziché SVF cellulare (cSVF) (Trivisonno et al. 2019).
Le funzioni della SVF sono alla base dell’interesse clinico per il tessuto adiposo. Numerosi studi hanno dimostrato che sia la SVF sia le cellule mesenchimali da essa derivate (ADMSCs) possono promuovere la guarigione e la riparazione dei tessuti tramite una combinazione di azioni chemiotattiche, paracrine e autocrine. In particolare, la SVF rilascia un ricco secretoma di fattori di crescita, citochine antinfiammatorie e pro-angiogeniche che stimolano la riparazione dei tessuti lesionati. Inoltre, le ADMSCs possono differenziarsi in vari lineaggi tissutali in determinate condizioni (osteogenico, condrogenico, angiogenetico…) ma soprattutto agiscono modulando l’infiammazione e favorendo la vascolarizzazione e la riepitelizzazione delle ferite. Un esempio interessante è il ruolo dei periciti della SVF: in presenza di infiammazione si staccano dai capillari e si trasformano in cellule mesenchimali attive, contribuendo a ridurre le citochine pro-infiammatorie e a orchestrare la riparazione tissutale. Le cellule contenute nella SVF sono in grado di percepire l’ambiente lesionato e rilasciare segnali che calmano l’infiammazione, stimolano la formazione di nuovi vasi sanguigni e supportano la riparazione dei tessuti (Trivisonno et al. 2019; Shimozono et al. 2021; Yaylacı et al. 2023; Arcani et al. 2025).
Micronizzazione
La micronizzazione è una tecnica meccanica di manipolazione minima per ridimensionare le particelle del tessuto adiposo, aspirato mediante tecnica di liposuzione a bassa pressione, allo scopo di ottenere la MAM (Matrice Adiposa Micronizzata): una sospensione emulsionata, omogenea e iniettabile in cui la matrice extracellulare è stata frammentata ma conservata e le ADMSCs, le cellule progenitrici e le citochine della frazione stromale sono state esposte. La MAM è ricca di cellule stromali vitali e fattori di crescita e viene ottenuta senza l’utilizzo di macchinari, enzimi o sostanze chimiche.
In particolare, la micronizzazione è un processo che viene eseguito interamente in campo sterile nel medesimo tempo chirurgico della lipoaspirazione. La tecnica prevede la lipoaspirazione, la purificazione del lipoaspirato e la sua successiva micronizzazione mediante l’utilizzo di micronizzatori in serie a porosità decrescente, dotati di migliaia di microlame, attraverso i quali viene fatto passare il lipoaspirato.
Questa tecnica permette di ridimensionare il tessuto adiposo, esponendo la SVF e le cellule in essa presenti, conservando parte della matrice extracellulare e mantenendo inalterata la vitalità cellulare.
La micronizzazione infatti, grazie alla capacità di conservazione della matrice extracellulare garantisce il mantenimento di un’elevatissima vitalità cellulare, anche nel lungo periodo, permettendo un effetto riparativo prolungato. Questo si traduce in una migliore attività secretoria da parte delle cellule stromali e quindi un prolungato e migliore effetto chemiotattico e paracrino.
Micronizzazione VS altre metodiche
I principali vantaggi della micronizzazione in campo sterile rispetto alla digestione enzimatica sono la sicurezza, la semplicità, la rapidità, i costi ridotti e l’aderenza ai requisiti normativi di “manipolazione minima” (Trivisonno et al. 2019; Yaylacı et al. 2023; Sowa et al. 2024/2025). Inoltre, la micronizzazione viene eseguita direttamente in sala operatori in campo sterile, il chirurgo stesso prepara il materiale e lo infiltra durante l’intervento. Il profilo di sicurezza è ottimo: nessuno strumentario esterno necessario oltre al kit sterile monouso e si parla di un trattamento autologo. Non vi è nessun residuo chimico e nessun evento avverso serio è stato riportato in studi clinici con iniezione di SVF meccanica, a parte lieve dolore o gonfiore transitorio. Anche il rischio di contaminazione è minimo, dato che i sistemi sono chiusi e sterili.
Un confronto tra sistemi di micronizzazione con filtri “blunt” a bordi smussi e con lame affilate ha rilevato una differenza modesta nel numero di cellule ottenute, a fronte però di cellule più integre in quelli con il taglio affilato, come i micronizzatori presenti nel kit J.A.K. (Copcu e Oztan 2020). Inoltre, è stato anche dimostrato che la tecnica di purificazione e successiva micronizzazione permette di ottenere un maggior numero di cellule nucleate della SVF rispetto alla centrifugazione.
Il numero di cellule nucleate ottenute con la micronizzazione è circa il 75%, con una conta di circa 2×107/ml di cellule per 1 ml di tessuto adiposo originario. La micronizzazione del tessuto adiposo permette di ottenere un maggior arricchimento di cellule progenitrici, sia libere sia legate alla matrice, garantendo un maggiore potenziale riparativo rispetto a quelle ottenute con la sola digestione enzimatica. (Yaylacı et al. 2023). Le cellule stromali così isolate si differenziano più velocemente e producono elevati livelli di marker di espressione genica rispetto a quelle isolate con la digestione enzimatica (Yaylacı et al. 2023; Sowa et al. 2024/2025).
È stato dimostrato che la micronizzazione è paragonabile alla digestione enzimatica in merito al numero di cellule progenitrici esposte, alla vitalità e al tasso di proliferazione, mentre la micronizzazione risulta più efficiente in termini di potenziale di differenziazione cellulare delle cellule stromali isolate (Trivisonno et al. 2019; Yaylacı et al. 2023).
Arcani et al. (2025) hanno anche paragonato vari sistemi per la processazione del tessuto adiposo e ciò che emerge è che la micronizzazione risulta essere un ottimo metodo in quanto a vitalità cellulare (>85%) e funzionalità cellulare; in particolare la micronizzazione permette di raccogliere una maggior proporzione di cellule stromali/staminali nella MAM ottenuta, avendo un valore biologico più alto rispetto ad altre metodiche che utilizzano l’emulsione. Inoltre, la MAM ottenuta con la micronizzazione non presenta detriti cellulari e frazione oleosa ma conserva la matrice extracellulare.
In sostanza, la micronizzazione offre un prodotto “pronto all’uso” con un buon bilancio tra quantità, qualità e vitalità cellulare, al contempo mantenendo elevato il livello di praticità e di conservazione della nicchia naturale del tessuto.
La micronizzazione può essere impiegata al posto del metodo enzimatico in termini di resa e vitalità cellulare, in particolare nelle applicazioni riparative, isolando rapidamente un’elevata percentuale di cellule progenitrici (Yaylacı et al. 2023).
J.A.K. – Joint Adipose Kit
J.A.K. è un kit assemblato pronto all’uso contenente tutto il necessario in confezione singola sterile per la preparazione di una MAM mediante la micronizzazione, partendo da un lipoaspirato autologo.
J.A.K. è studiato per ottenere una MAM purificata, micronizzata a viscosità modulabile e in cui vengono preservate la vitalità cellulare e la struttura della matrice extracellulare nell’ottica del mantenimento della funzionalità cellulare.
All’interno del kit non si trovano le cannule per tumescenza e lipoaspirazione che vengono fornite a parte, pluriuso e risterilizzabili. Le cannule fornite sono dotate di attacco super luerlock per una buona tenuta con la siringa in aspirazione. La cannula per la lipoaspirazione è lunga 20 cm e dotata di 20 fori da 1 mm di diametro, per consentire una buona raccolta di tessuto adiposo con cluster ridotto.
REF:JAK-600
La procedura è molto semplice e rapida e prevede pochi passaggi, standardizzati, minimamente operatore dipendenti, tutti in campo sterile, senza l’utilizzo di sostanze chimiche o macchinari.
Le fasi di utilizzo sono tre: (1) raccolta, (2) purificazione e (3) micronizzazione.
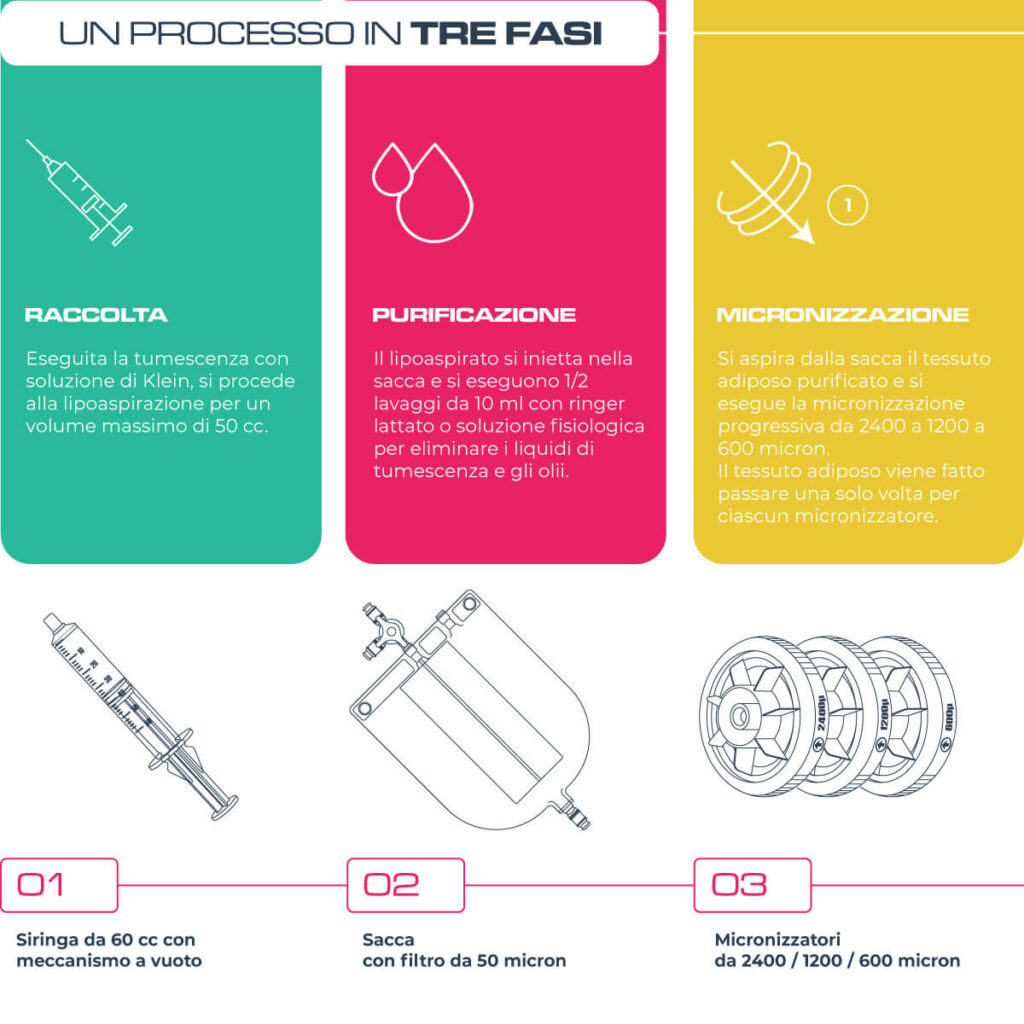
1. Raccolta
La raccolta del lipoaspirato avviene mediante normale processo di liposuzione con tecnica sottovuoto a bassa pressione, con precedente tumescenza con soluzione di Klein.
Successivamente vengono eseguite la purificazione e la micronizzazione.
2. Purificazione
La purificazione avviene in una sacca sterile appositamente studiata per questa funzione, dotata di filtro interno da 50 µm che trattiene il tessuto adiposo e permette l’eliminazione dei residui ematici, di tumescenza e della frazione oleosa, mediante lavaggio con ringer lattato sterile o, in assenza, soluzione fisiologica sterile. Si ottiene così un lipoaspirato purificato da tutte le componenti pro-infiammatorie che potrebbero causare un rapido riassorbimento della MAM iniettata nella sede da trattare.
In seguito, il tessuto adiposo viene estratto e micronizzato in 3 rapidi passaggi sequenziali.
3. Micronizzazione
I micronizzatori utilizzati nel kit J.A.K. sono 3, dotati di porosità decrescente: 2400 µm (rosa), 1200 µm (verde) e 600 µm (giallo). I 3 micronizzatori possono essere utilizzati in sequenza per avere il massimo del ridimensionamento, del rilascio cellulare e della micronizzazione del tessuto adiposo oppure ci si può fermare all’utilizzo del primo o dei primi due per ottenere una MAM più densa e strutturata. Il Medico può quindi scegliere la viscosità della MAM da iniettare.
I micronizzatori utilizzati nel kit J.A.K. sono stati selezionati per ottenere una MAM emulsionata, omogenea, facilmente iniettabile e ricca di cellule stromali vitali, fattori di crescita e matrice extracellulare.

I micronizzatori sono dotati di migliaia di microlame esagonali e parallele, disposte su un’ampia superficie, in modo tale da microframmentare il tessuto senza esercitare forti pressioni contusive e senza ledere la vitalità cellulare e la struttura della matrice extracellulare (Yaylacı et al. 2023).
I micronizzatori sono dotati di verso per il passaggio del tessuto adiposo, contrassegnato dalla freccia nera sul bordo. È sufficiente un singolo passaggio per ogni micronizzatore, in sequenza decrescente, per ridimensionare, emulsionare e omogeneizzare il tessuto adiposo. Per un sicuro attacco sono dotati di connessione luerlock.
La micronizzazione avviene sempre secondo una metodica standard, rapida e sicura, completamente in campo sterile.

Applicazioni cliniche della MAM
Grazie alle sue proprietà antinfiammatorie e pro-riparative, il tessuto adiposo micronizzato è stato utilizzato in diverse applicazioni cliniche, spesso come trattamento per condizioni degenerative o di difficile guarigione.
Osteoartrosi del ginocchio
Numerosi studi pilota, sia in combinazione con interventi chirurgici che come trattamento infiltrativo standalone, hanno riportato esiti positivi in termini di riduzione del dolore e miglioramento della funzione del ginocchio. Russo et al. (2018) attestano che pazienti trattati con MAM per osteoartrosi di ginocchio hanno conservato, dopo 3 anni, il miglioramento clinico ottenuto a 12 mesi senza effetti avversi rilevanti. Zannoni et al. (2024) riportano un miglioramento significativo nella sintomatologia dolorosa e nella funzionalità articolare a 12 mesi dal trattamento infiltrativo, senza effetti avversi e complicanze.
Shimozono et al. (2021) hanno trattato casi di artrosi post-traumatica della caviglia combinando debridement artroscopico e iniezione di MAM. A circa 14 mesi di distanza, hanno osservato un miglioramento medio del dolore VAS da 6,1 a 3,8 e incrementi significativi nei punteggi FAOS di dolore e qualità di vita (da ~49 a 61 e da 20 a 30 rispettivamente). I pazienti con artrosi meno avanzata (grado 3) rispondevano meglio di quelli in stadio più severo (grado 4).
Anche Holzbauer et al. (2024) confermano che il tessuto adiposo micronizzato porta ad un significativo miglioramento clinico nei pazienti con osteoartrosi di ginocchio.
I risultati espressi dagli studi riguardanti l’iniezione di MAM per il trattamento dell’osteoartrosi evidenziano come il tessuto adiposo micronizzato agisca a livello di:
- Riduzione del dolore: la maggior parte degli studi ha riportato una significativa diminuzione dei livelli di dolore, misurata tramite scale come il Visual Analogue Scale (VAS).
- Miglioramento funzionale: i pazienti hanno mostrato miglioramenti nei parametri funzionali, inclusi punteggi come KOOS (Knee Injury and Osteoarthritis Outcome Score) e WOMAC (Western Ontario and McMaster Universities Osteoarthritis Index).
- Miglioramento dello stato della cartilagine: in alcuni studi, l’uso di MAM ha mostrato segni di riparazione della cartilagine, confermati da esami radiologici (MRI) e, in alcuni casi, da artroscopie di controllo.
- Sostenibilità dei risultati: i benefici clinici e radiologici sono stati osservati fino a 2-3 anni di follow-up, con alcuni studi che hanno evidenziato una stabilizzazione o miglioramento delle condizioni articolari.
Le iniezioni intra-articolari di MAM rappresentano un’opzione promettente per ridurre i sintomi dell’osteoartrite del ginocchio e favorire la riparazione della cartilagine, con risultati sostenibili nel medio termine.
Ulcere cutanee diabetiche e ferite difficili
Le ulcere del piede diabetico e le ferite croniche di difficile guarigione rappresentano un altro campo di applicazione per la MAM. In ambito di chirurgia plastica si è osservato che il lipofilling in ulcere refrattarie può portare a miglioramenti.
Feng et al. (2015) riferiscono una rapida riepitelizzazione e una migliore granulazione del tessuto cutaneo in ulcere del piede diabetico, con la chiusura completa dell’ulcera in un elevato numero di pazienti rispetto al trattamento standard.
Questi risultati indicano che la componente stromale della MAM può contribuire a rivitalizzare tessuti cronicamente ischemici, promuovendo angiogenesi e modulando l’infiammazione locale. Va sottolineato che nelle ulcere diabetiche avanzate spesso coesistono infezioni e gravi problemi vascolari; la MAM può essere un utile coadiuvante nel contesto di un trattamento multidisciplinare (sbrigliamento chirurgico, antibiotici, scarico pressorio, ecc.).
Lesioni nervose periferiche
Un campo emergente di applicazione è quello delle lesioni dei nervi periferici. La capacità rigenerativa intrinseca dei nervi adulti è molto limitata nel caso di perdite di sostanza di tratti lunghi, per cui spesso si ricorre a tubi di conduzione (conduit) o innesti nervosi. Il tessuto adiposo micronizzato viene utilizzato come materiale bioattivo inserito all’interno dei tubi di conduzione artificiale, in modo da fornire fattori trofici e cellule di supporto alla ricrescita delle fibre nervose. Uno studio sperimentale pubblicato su Plastic and Reconstructive Surgery (Sawai et al. 2023) ha esaminato questo approccio in un modello animale: ratti con un gap nel nervo sciatico colmato da un tubo di silicone in cui è stato iniettata MAM autologa. I risultati mostrano che l’aggiunta di MAM ha accelerato la rigenerazione nervosa rispetto ai tubi senza, con un recupero migliore della funzione. In particolare, la densità di fibre mielinizzate attraverso il gap e la velocità di conduzione nervosa erano superiori nel gruppo con adiposo micronizzato, indicando una rigenerazione più efficace. Gli autori concludono che la MAM è un materiale promettente per il trattamento di lesioni nervose periferiche in quanto potenzia l’effetto dei conduit artificiali.
Dal lato clinico questo approccio è ancora ai primi passi ma la MAM è stata utilizzata per iniezioni attorno ai nervi periferici per il trattamento delle neuropatie da intrappolamento, grazie al suo effetto antinfiammatorio.
Inoltre, in chirurgia ricostruttiva è stato osservato che l’innesto di MAM nelle zone di lesione nervosa può migliorare il trofismo locale e facilitare il recupero. I dati preclinici come quelli di Sawai et al. (2023) supportano questa direzione, mostrando concretamente che le cellule stromali della MAM rilasciano fattori che stimolano la ricrescita assonale e la rimielinizzazione.
Altre possibili applicazioni
Oltre ai campi sopra menzionati, la letteratura suggerisce molte altre possibili applicazioni della MAM autologa. In ortopedia sono stati avviati studi su patologie tendinee (tendiniti croniche, lesioni della cuffia dei rotatori) trattate con iniezioni di MAM con l’idea di promuovere la riparazione dei tendini degenerati. In campo cardiologico, sono in corso ricerche sull’uso di MAM autologa per il trattamento dell’ischemia miocardica cronica e dello scompenso cardiaco: le cellule adipose possono infatti favorire la neovascolarizzazione del muscolo cardiaco post-infarto. Sul versante delle malattie autoimmuni, si è ipotizzato di utilizzare le proprietà immunomodulanti delle ADMSCs contenute nella MAM per condizioni come l’artrite reumatoide o il lupus.
Un’altra applicazione clinica interessante è nel trattamento delle fistole perianali complesse, soprattutto nei pazienti con Malattia di Crohn. Il trattamento con MAM prevede l’iniezione nel dotto fistoloso e anche nella zona peri-fistolosa. Nel caso di fistole complesse con più dotti potrebbero essere necessarie più applicazioni prima di ottenere la completa chiusura dei tramiti ma nel mentre si osserva un deciso e più rapido miglioramento rispetto ai trattamenti senza l’utilizzo di MAM autologa.
In ambito estetico e dermatologico, infine, la MAM viene spesso impiegata per migliorare la qualità della pelle (ringiovanimento del viso, trattamento di cicatrici e radiodermiti) grazie alla capacità delle cellule stromali di stimolare la produzione di nuovo collagene e vascolarizzare i tessuti cutanei danneggiati (Trivisonno et al. 2019).
CONCLUSIONI
Allo stato attuale (2025), l’uso di tessuto adiposo micronizzato rappresenta una frontiera promettente della medicina rigenerativa, con un profilo di sicurezza molto buono, una bassa morbilità, elevata concentrazione e vitalità cellulare e risultati clinici incoraggianti in vari campi: dal trattamento della sintomatologia dolorosa dell’osteoartrosi, alla guarigione di ferite difficili, al trattamento dermatologico, proctologico e alla rimielinizzazione nelle lesioni nervose.
In particolare, il kit J.A.K. è un sistema sicuro, facile e veloce per ottenere in modo standardizzato una MAM autologa purificata a viscosità modulabile, funzionale per tutte le applicazioni possibili. Infatti, a seconda del distretto anatomico da trattare la presenza di 3 micronizzatori a porosità decrescente consente la modulazione del ridimensionamento della MAM rendendola sempre facilmente applicabile e rispondente alle necessità del Medico.
Redazione scientifica: Dott.ssa Carlotta Boschian.
